以前Math 2やPhysicsの記事を書きましたが、今回はSAT Subject Testのもう一つの(理系の)主要科目とも言えるChemistry(化学)について話していきたいと思います。SAT Chemistryを受験する人の多くは生物系・化学系の専攻を目指している人ですが、文系でChemistryを受ける人も多い印象です。
試験範囲

文系で化学基礎までしか履修していない場合と理系化学を履修した場合に分けて、SAT Chemistryの範囲と日本の(中学と)高校のカリキュラムを比較してみました。理系化学が一通り終わっている場合、SAT Chemistryの範囲のほとんどに対応できるということが分かると思います。一部最初の方で量子力学や原子軌道の知識が必要だったり、熱化学の分野で普段慣れていない記号やギブスの自由エネルギー、エントロピーなどの言葉出てきたりします。これらのトピックは有機化学をやる時に「発展」の内容として扱われることが多く、実際(僕が知っている限り)日本の大学入試に直接出題されることはありません。しかし、僕が1年の1学期に一般化学を履修した時、高校でこれらのトピックを学習した前提で授業が行われ、復習範囲として最初の週に少し触れた程度なので、アメリカの大学で化学を必要とするような学問(一部の工学専攻、生物・化学系など)を専攻したい場合は、SAT Chemistryを機にこれらを勉強するのも良いと思います。また、量子力学と聞いて難しいというイメージがあるかもしれませんが、少なくともSAT Chemistryなどに出る問題ではシュレディンガー方程式を解くことを必要とするものなどの高度な問題は出題されないので、独学でも全然対応可能です(もちろんオービタルなどの形はシュレディンガー方程式を解かないと導出できないという点はありますが、ここでは概念だけ知っていれば十分です)。文系で化学基礎までしか履修していなくても、同様にそこまで高度な数学などは必要ないので、独学でも対応できた方は多くいるようです。特に、文系だが理系科目のSubject Testを少なくとも1つ取っておきたい、という人はSAT PhysicsよりChemistryを選ぶ場合が多い印象です。
試験形式・例題
1時間で85問の選択肢問題を解きます。計算機は使用不可、周期表が与えられるという特徴があります。また、問題は主に次の3つの種類があります:
- Classification:選択肢が複数与えられて、その後の問題に最も適しているものを選ぶ。
- Relationship Analysis:〜because〜という形の問題。”because”の前の文とその後の文がそれぞれ正しいかを判定し、更に2つ目の文が1つ目の文の説明になっているかどうかを答える。
- 5-Choice Completion Questions:一般的な選択肢問題
まず、Classification問題の例を見ていきましょう(全ての問題はCollege Boardより):
問題:Reacts with an equal volume of 0.05 M Ba(OH)2 to form a solution with pH = 7:
選択肢:A) 0.1 M HCl B) 0.1 M NaCl C) 0.1 M HC2H3O2 D) 0.1 M CH3OH E) 0.1 M KOH
この問題は一応”Hard”という難易度を付けられていますが、酸と塩基をしっかり理解していればすぐ答えられると思います。特に、水酸化バリウムBa(OH)2が強塩基であるという知識があれば、あとは1Lの水酸化バリウムに対して濃度が0.05 Mであることより水酸化物イオンOH–がができるので同じく1Lに対して0.1 molの水素イオンをくれる溶液を探すという方針が出てくると思います。ここで、C)の酢酸は弱酸なのでpH>7になるので、答えは強酸であるA)の塩酸HClになります。
※ちなみに、高校化学ではmol/Lを使うと思いますが、SATなどにはM(モーラー・モル)という単位が出てきます。mol/L = Mです。
では、Relationship Analysisの問題:
問題:
[I] Diamond has a high melting point
BECAUSE
[II] in a diamond crystal, the carbon atoms are held in place by ionic bonds.
これは結構知識問題っていう側面が強い気がしますが、ダイアモンドは確かに融点が高い(3550度以上)ので、[I]はTrueです。しかし、ダイヤの炭素原子はイオン結合ではなく、共有結合で結ばれているので[II]はFalseです。これも知識で答えられますが、イオン結合は電気陰性度の差が大きい原子同士、共有結合は電気陰性度が近いもの同士で起こるということから答えを「導く」こともできます。ちなみに、今回は明らかですが、という式(ここで、
はそれぞれの電気陰性度)からイオン結合か共有結合に近いかを判断することもできます。最後に、[II]は[I]の説明になっていない(そもそも正しくない)のでCE (Correct Explanation)ではないです。
3つ目の種類の問題は、一般的な選択肢問題です。例題を見ていきましょう:

水素14%、炭素86%と言われているので取り敢えず比をとると、になります。実際の試験では周期表が使えるので覚える必要はありませんが、原子量がそれぞれC=12, H=1(問題を解くうちに覚えている場合が多いですね)であることにより、mol(物質量)の比に変えると
なので組成式(empirical formula)はCH2です(選択肢B)。問題に分子量が与えられていないので、エチレン(C2H4)である可能性はありますが、100%そうとは言えないのでC)とD)を外します。A)は一応間違っていはいないですが、確認したところ模範解答はBと言っています。これは、多分”most informative statement”を選ばなければいけないということが理由であると考えられます。
日本の高校化学ではあまり扱われない電子配置の話に関する基本的な問題も載せておきます:
問題:Has electron configuration
選択肢:A) Ar B) O C) S D) TI E) U
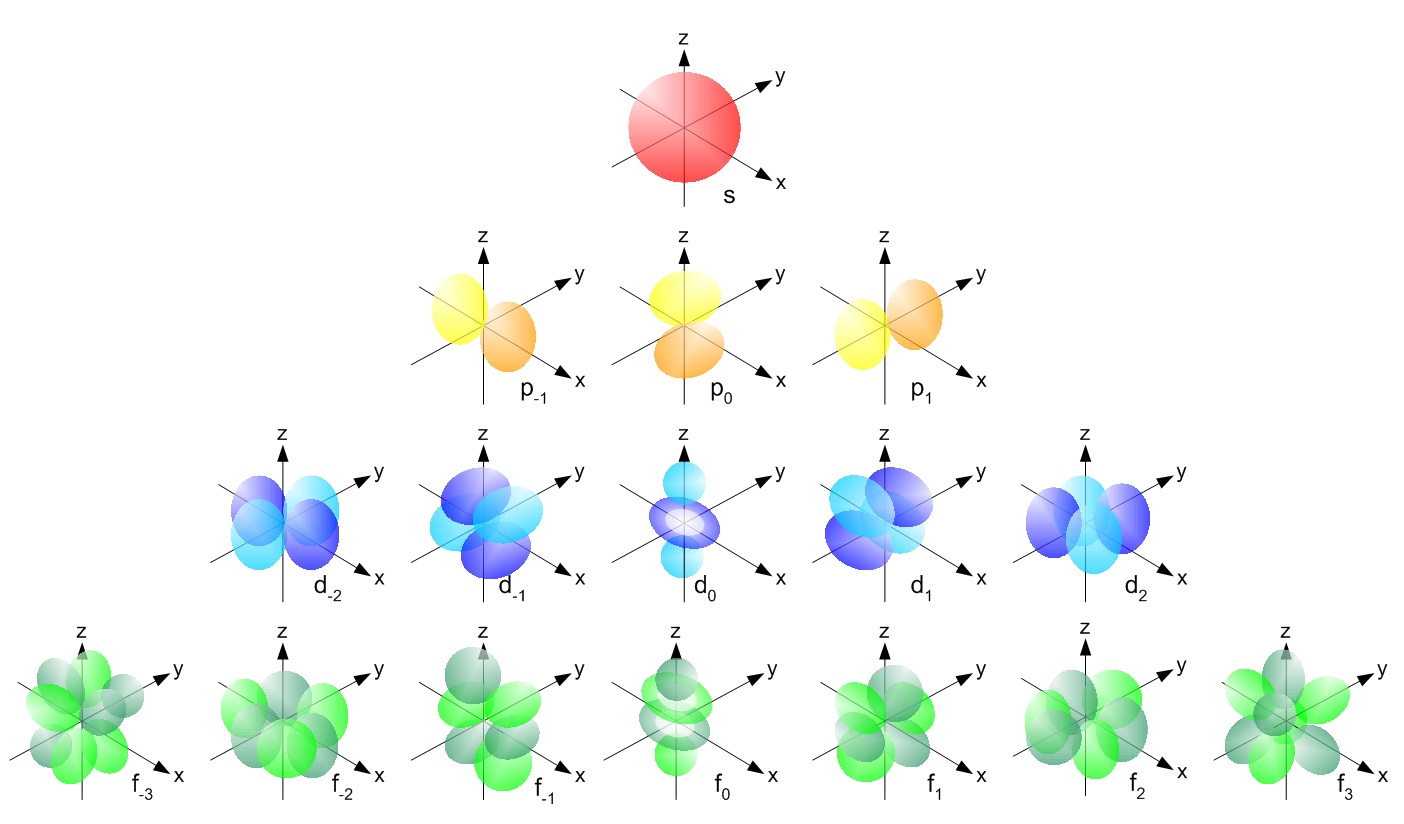
ここで簡単に電子軌道の説明をすると、中学・高校では電子が原子核の周りの軌道を回っている(ボーア模型)と学びますが、実は電子はエネルギーが異なる電子軌道というものに入っています。問題文に出てきているsとpはそれぞれ球、亜鈴状の形の軌道で、電子がそこにあるかもしれない確率と関係しています。
余談:厳密に言うと、軌道はシュレディンガー方程式から出てきた波動関数で、その二乗が確率密度を表しています。例えば、水素原子の1s軌道(基底状態)の場合、シュレディンガー方程式 (
はハミルトニアン(力学的エネルギー)と言う演算子で、
はエネルギー準位)から出てきた波動関数は極座標では
で、2乗すると
と言う確率密度が出てきます。ここで、
はボーア半径と呼ばれます。これは球面座標系における動径
にしか依存しないので、1s軌道が球の形をしているのが分かると思います(実際の確率は
になります)。ちなみに、p軌道(例えば
)は
と言うもう少し複雑な式で表されます。
ただ、少なくともSAT Chemistryの問題に限っては、このような知識はそこまで必要ありません。電子が低エネルギーの軌道から入り(構造原理・Aufbau Principle)、各軌道に最大2個の(スピンが異なる)電子が入れて(パウリの禁止律)、同じエネルギーの軌道に入る場合はまずスピンの方向が同じ向きになるように入る(フントの法則)ということを知っていると、あとは3()と言う数字から第3周期にあり、M殻(
)に電子が
個あるので原子番号16番の硫黄S(選択肢C)を選べると思います。
対策法・勉強法
他の試験の対策の記事でも書いていますが、SAT Subject Test系の試験対策は基本的に:
- Barron’s, Princeton Reviewなどの参考書1冊
- The Official SAT Subject Test Study Guide(今回はもちろんChemistry版)
の2冊で十分だと思います。オービタルなどの未習範囲については、ネットに色々講義ノートや動画が載っているので、それを参考にして勉強し始めるのも良いかもしれません。また、英語に自信があるならば、直接Barron’sの参考書を読むのでも十分だと思います。他のSubject Testと同様、やはり一番のハードルは実際の内容ではなく、問題を英語で素早く理解し、解く必要があるという点です。英語のレベルにもよりますが、やはりどのレベルでも、日頃から重要な専門用語の英訳を調べたり、単語帳を使ったりするのが効果的なのではないかと思います。











